Penicilliner
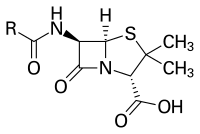
De penicilliner eller penicilliner (singular penicillin , från latin Penicillium , ' borste mold ') är en grupp av antibiotiska substanser som strukturellt är härledda från 6-aminopenicillansyra . Förutom naturligt förekommande penicilliner, som bildas som sekundära metaboliska produkter av olika Penicillium- , Aspergillus- , Trichophyton- och Streptomyces -arter , inkluderar detta även biosyntetiskt och delvis syntetiskt producerade penicilliner. Det naturligt förekommande penicillinet som upptäcktes först isolerades från penselformen Penicillium notatum .
Penicillin G , ett naturligt penicillin som fortfarande används terapeutiskt idag, är ett av de äldsta antibiotika som används , vilket förutom sin stora medicinska fördel också tilldelas en pionjärroll i den vetenskapliga användningen av denna grupp aktiva ingredienser. Efter återupptäckten av penicillins antibiotikaeffektivitet, erkänd och publicerad av Theodor Billroth 1874, av Alexander Fleming 1928, erkändes den enorma betydelsen av antibiotika för medicin , vilket väsentligt har påverkat och revolutionerat den moderna förståelsen av betydelsen av bakteriella patogener. . Under årtiondena efter upptäckten hjälpte penicillin G till att rädda otaliga liv. Även om det idag finns många bakteriestammar som är resistenta mot detta antibiotikum, kan det fortfarande användas framgångsrikt runt om i världen.
Penicilliner tillhör gruppen β-laktamantibiotika . Den empiriska formeln är RC 9 H 11 N 2 O 4 S, där “R” står för en variabel sidokedja.
Klassificering
Naturligt förekommande penicilliner
Modersubstansen för penicilliner, 6-aminopenicillansyra, härstammar biologiskt från L-α-amino- adipinsyra och aminosyrorna L- cystein och L- valin , varigenom isopenicillin N initialt bildas. Ersättningen av L-a-aminoadipylresten med andra organiska syrarester, katalyserad av acyltransferas , resulterar i olika penicilliner. Av de naturliga penicillinerna är endast penicillin G ( bensylpenicillin ), som erhålls genom jäsning från Penicillium chrysogenum , terapeutiskt signifikant . Det bryts inte ner lika snabbt som det mer effektiva penicillinet K. Med hjälp av en lämplig föregångare , fenylättiksyra , kan det också framställas specifikt genom jäsning. Förutom Penicillium -arter som biologiska producenter bildas penicilliner också av andra mögel som Acremonium chrysogenum (tidigare Cephalosporium acremonium ) och Aspergillus nidulans , samt av vissa bakterier som tillhör ordningen Actinomycetales , till exempel Streptomyces clavuligerus producerar penicillin N.
| Efternamn | Andra namn | aktivitet | -R | Molekylär formel | Molmassa | CAS-nummer | PubChem |
|---|---|---|---|---|---|---|---|
| Penicillin F. | Penicillin I, penten (2) yl-penicillin | 1500 IE / ml | -CH 2 -CH = CH-CH 2 -CH 3 | C 14 H 20 N 2 O 4 S | 312,38 g · mol -1 | 118-53-6 | 6438232 |
| Penicillin G. | Penicillin II, bensylpenicillin | 1670 IE / ml ( natriumsalt ) | -CH 2 -C 6 H 5 | C 16 H 18 N 2 O 4 S | 334,39 g · mol -1 | 61-33-6 | 5904 |
| Penicillin X | Penicillin III, p-hydroxibensylpenicillin | 850-900 IE / ml | -CH 2 -C 6 H 4 -OH | C 16 H 18 N 2 O 5 S | 350,39 g · mol -1 | 525-91-7 | 120720 |
| Penicillin K | Penicillin IV, heptylpenicillin | 2200 IE / ml | -CH 2 -(CH 2 ) 5 -CH 3 | C 16 H 25 N 2 O 4 S | 341,45 g · mol -1 | 525-97-3 | 44123577 |
| Penicillin DF | Dihydropenicillin F, penicillin H 2 F, amylpenicillin | 1610 IE / ml | -CH 2 -(CH 2 ) 3 -CH 3 | C 14 H 22 N 2 O 4 S | 314,40 g · mol -1 | 4493-18-9 | 107556 |
| Penicillin N | Adicillin | - (CH 2 ) 3 -CH (NH 2 ) COOH | C 14 H 21 N 3 O 6 S | 359,40 g · mol -1 | 71724 | ||
| Penicillin M. | Isopenicillin N | - (CH 2 ) 3 -CH (NH 2 ) COOH | C 14 H 21 N 3 O 6 S | 359,40 g · mol -1 | 440723 | ||
Bio- och delvis syntetiska penicilliner
Det oralt effektiva penicillinet V ( fenoximetylpenicillin ) produceras också fermentativt, men inte spontant, utan genom tillsats av en syntetisk föregångare , fenoxiättiksyra ("biosyntes").
Delvis syntetisk vidareutveckling av de naturliga penicillinerna är resultatet av reaktionen mellan 6-aminopenicillinsyra och karboxylsyrahalogenider . De har vissa fördelar jämfört med penicillin G, såsom syra och penicillinas stabilitet eller ett utökat spektrum av aktivitet.
Syrastabila (oralt effektiva) penicilliner med eller utan penicillinasstabilitet
- Fenoximetylpenicillin (penicillin V), propicillin , feneticillin
På grund av den reducerade nukleofilicitet hos det karbonylsyre , attack av hydroniumjoner är joner försvåras, vilket betyder att omvandlingen till den ineffektiva penillic syran inhiberas. Syrstabila penicilliner förstörs inte av magsyra och kan därför administreras oralt . De har samma aktivitetsspektrum som penicillin G.
Penicillinas-stabila penicilliner
Genom att skydda beta-laktamringen med isoxazolylstrukturer från penicillinas som bildas av vissa patogener , är sådana penicilliner också effektiva mot penicillinasbildande stafylokocker ("stafylokockpenicillin"). Jämfört med penicillin G är deras styrka betydligt lägre och isoxazolylpenicilliner är helt ineffektiva mot gramnegativa patogener.
Penicilliner med brett spektrum
- Aminopenicilliner : Amoxicillin , Ampicillin , Bacampicillin , Pivampicillin , Sultamicillin
- Karboxipenicilliner: karbenicillin , ticarcillin
- Ureidopenicilliner (acylaminopenicilliner): azlocillin , piperacillin , mezlocillin
Genom att införa polära substituenter kan sådana hydrofila penicilliner passera genom cellväggarna hos gramnegativa patogener och därmed utöka deras spektrum av aktivitet. Bredspektrumpenicillinerna är dels syra- och penicillinaskänsliga, dels minskar deras effektivitet mot vissa grampositiva bakterier också.
Pivmecillinam är inte en acyleringsprodukt av 6-aminopenicillansyra, men den har den bicykliska laktam-ryggraden i penicilliner.
farmakologi
Handlingsmekanism
Penicilliner har en bakteriolytisk effekt på celldelningen av bakterierna , nämligen när cellväggen byggs om genom att ingripa i cellväggens syntes, förhindrar den inre tvärbindningen där och försvagar därmed cellväggen så att den spricker när den utsätts för stress. Särskilt grampositiva bakterier som delar sig dör under påverkan av penicillin. Den grundläggande strukturen för penicilliner består av 6-aminopenicillansyra, en bicyklisk dipeptid gjord av cystein (L-konfigurerad) och valin (D-konfigurerad, efter konfigurationsomvändning i den biosyntetiska vägen). Denna så kallade beta-laktamring är (när den är öppen) bunden av bakterieenzymet D-alanintranspeptidas , som ansvarar för tvärbindning av peptidoglykanerna i bakteriecellväggarna hos grampositiva bakterier. Enzymet krävs huvudsakligen för att dela bakterier, eftersom i dessa måste den styva cellväggen öppnas och åtminstone delvis re-syntetiseras. Eftersom bindningen till D-alanintranspeptidas är oåterkallelig kan cellväggen inte längre syntetiseras och den grampositiva bakterien förlorar sin viktigaste skyddande täckning. Dessutom leder den konstanta uppbyggnaden och nedbrytningen av den defekta cellväggen till giftiga nedbrytningsprodukter.
Effekten av penicilliner påverkar bara bakterier som förökar sig, men inte de som inte delar sig: Dessa påverkar inte längre antibiotikumet eftersom ingen ny cellväggssyntes behöver äga rum - det är redan helt komplett och bildar därför inte längre en attackpunkt för penicillin. Bakterier som inte förökar sig utgör dock inget hot för värdorganismen och görs relativt ofarliga relativt snabbt av patientens eget immunsystem. Om de å andra sidan går in i en reproduktionscykel, bryts cellväggen igen delvis ner och måste syntetiseras på nytt; sådana bakterier kan därför attackeras igen av penicilliner. Av denna anledning måste penicilliner fortsätta att administreras under en viss period efter att symtomen har avtagit.
Penicilliner är bara effektiva om bakterierna annars är obehindrade i sin tillväxt; så penicilliner ska inte administreras tillsammans med läkemedel som hindrar bakterierna från att föröka sig, annars blockeras utgångspunkten för penicillins verkningsmetod terapeutiskt.
Penicilliner inte bara verkar på bakterier, innefattande cyanobakterier , men också blockera fördelningen cyanelles, de fotosyntetiskt aktiva organeller av den Glaucocystaceae (en familj av alger) och kloroplasterna av blåsan mossa . Men , de har ingen effekt på fördelningen av plastider i högre utvecklade kärlväxter som tomater . Detta är en indikation på att β-laktamantibiotika i allmänhet inte längre har någon effekt på kloroplaster på grund av evolutionära förändringar i plastiddivisionen.
Penicillin G och V är inte effektiva mot gramnegativa bakterier (med undantag för gramnegativa kocker som Neisseria ), som har ytterligare ett yttre membran över cellmembranet. Detta gör det omöjligt för penicillinet att attackera, eftersom det måste ingripa i bildandet av peptidoglykanskiktet nedan. Därför är användningen av penicillin G och V bara meningsfull med grampositiva bakterier. Strukturella varianter som aminopenicilliner används mot gramnegativa bakterier .
Motstånd
Många - men inte alla - kliniskt förekommande bakterier är nu redan resistenta mot penicillin G , vilket har lett till ett antal avancerade β -laktamantibiotika. Ett undantag är bakterien Treponema pallidum (orsakande medel för syfilis / syfilis), mot vilken det ännu inte har utvecklats någon resistensutveckling mot penicilliner.
Problemet med korsresistens är fortfarande kritiskt, vilket innebär att bakterier som en gång har utvecklat resistens mot penicilliner också blir okänsliga för andra β-laktamantibiotika (t.ex. cefalosporiner ).
Motståndskraftiga mutanter skulle faktiskt inte göra någon skada, eftersom de bara förekommer i liten utsträckning. Men om penicillinet verkar på de andra, icke-resistenta bakterierna och eliminerar dem, kan en resistent bakterie reproducera sig mycket bättre och blir därmed en fara, eftersom den vidarebefordrar dess resistens till efterföljande generationer. Genom att utbyta resistensgener mellan olika typer av bakterier överförs antibiotikaresistens också till andra typer. Meticillinresistens är särskilt fruktad i Staphylococcus aureus .
Resistensutvecklingsprocessen är ett mycket tydligt exempel på Darwins evolutionsteori ( naturligt urval ); På grund av den snabba uppdelningen och successionen av generationer väljs de resistenta bakterierna anpassade till sin miljö ut och utgör grunden för senare generationer. Bildandet av penicillinresistenta stammar anses vara ett av de första experimentella bevisen på observerad mikroevolution . Den biologiska grunden för gruppen aktiva substanser är konkurrensen mellan de två organismstammarna svampar och bakterier, som förlitar sig på samma resurser, varigenom svamparna skyddar sig mot bakterierna med antibakteriella tillväxthämmande ämnen.
Bieffekter
Som med alla antibiotika kan resistens mot penicilliner också utvecklas. Frekvensen av allergier mot penicillinbehandling är mycket lägre än tidigare antaget (). Allergiska reaktioner kan sträcka sig från lätt rodnad i huden till anafylaktisk chock .
Penicilliner kan döda fördelaktiga bakterier som de i tarmfloran , särskilt bredspektrumpenicilliner, som också är effektiva mot gramnegativa bakterier. I värsta fall kan skadliga mikroorganismer sprida sig i tarmen och leda till antibiotikarelaterad kolit .
En annan sällsynt (med en sannolikhet på cirka tre promille) oönskad effekt är utlösande av epileptiska anfall .
berättelse
upptäckt

Redan 1874 hade kirurgen Theodor Billroth i Wien otvetydigt insett den bakterietillväxthämmande effekten av svampen Penicillium. År 1923, i San José, undersökte Clodomiro Picado Twight , en tidigare forskare vid Pasteur-institutet , de tillväxthämmande effekterna på stafylokocker och streptokocker . Hans forskningsresultat publicerades 1927 av Société de Biologie i Paris. (Åter) upptäckten av penicilliner med mycket mer publicitet började med en möglig bakteriekultur ett år senare: Alexander Fleming , som studerade stafylokocker vid St. Mary's Hospital i London , ympade en agarplatta med stafylokocker före sommarlovet 1928 och lägg den sedan åt sidan. När han kom tillbaka upptäckte han den 28 september 1928 att en mögel ( Penicillium notatum ) växte på näringsmediet och att bakterierna inte hade förökat sig i närheten av svampen. Fleming kallade det bakteriedödande ämnet som kunde extraheras från näringsmediet penicillin och beskrev det först för allmänheten 1929 i British Journal of Experimental Pathology . Han undersökte effekten av penicillin på olika typer av bakterier och djurceller ; Han fann att penicillin bara dödade grampositiva bakterier som stafylokocker, streptokocker eller pneumokocker , men inte gramnegativa bakterier som salmonella . Det visade sig också vara giftfritt för vita blodkroppar och mänskliga celler eller för kaniner. Trots denna kunskap fick Fleming tydligen aldrig idén att använda penicillin som läkemedel.
Nästan tio år senare, 1938, bestämde Howard W. Florey , Ernst B. Chain och Norman Heatley sig för att systematiskt undersöka alla ämnen som produceras av mikroorganismer som var kända för att vara skadliga för bakterier. Så här kom de över Flemings penicillin. De rengjorde den och undersökte dess terapeutiska effekter först på möss och sedan även på människor. 1939, René Dubos av den Rockefeller Institute for Medical Research isolerade tyrotricin från jordprover och visade att det hade förmågan att bota vissa bakterieinfektioner. Florey and Chain genomförde det första kliniska testet i Oxford 1941, men det var begränsat till endast ett fåtal personer. Eftersom produktionen av penicillin fortfarande var mycket mödosam, återhämtade de till och med urinen från de behandlade personerna.
Med början av andra världskriget ville de allierade utveckla ett effektivt läkemedel för sina sårade soldater. Antibiotisk forskning flyttade till USA och tog fart där i snabb takt. Det visade sig att det är billigare att odla svampen i lämpliga flytande näringsmedier. I USA, där små mängder penicillin redan hade producerats 1940 för behandling av syfilis bland draftees , uppföddes nya stammar av Penicillium chrysogenum , vilket producerade mer penicillin. Ämnet var således tillgängligt som ett läkemedel i erforderlig mängd. Penicillin användes först på de skadade 1942 av de allierade. År 1943 visade det sig att penicillin inte är ett kemiskt enhetligt ämne: Det råa penicillin som de brittiska forskarna erhöll genom ytlig jäsning (nedsänka jäsning) bestod främst av penicillin F, medan det råa penicillin som producerades i USA genom nedsänkt jäsning huvudsakligen bestod av av penicillin G. Totalt fyra varianter erkändes tidigt, vilka med romerska siffror betecknades som penicillin I, II, III och IV eller med bokstäverna F, G, X och K.
År 1945 fick Fleming, Chain och Florey tillsammans Nobelpriset för sin upptäckt som markerade en vändpunkt i medicinens historia. Den aktiva ingrediensen avslutade det medicinska problem som funnits sedan antiken att kirurgiska skador på grund av enkla sårinfektioner kan leda till att de drabbade dör långt efter kriget och därför fortfarande betraktades av befolkningen som ett mirakelmedicin efter kriget. I Tyskland låg fokus på vidareutvecklingen av sulfonamiderna , som fortfarande används i begränsad utsträckning idag , eftersom Allied Control Council inte hade tillåtit användning av penicillin i forskning eller medicinska tillämpningar. Det var inte förrän 1946 som en stam av penicillin kom till det Stolberg-baserade företaget Chemie Grünenthal under ytterst oförklarliga omständigheter , där produktionen började. Det tidigare importerade penicillinet blev allmänt tillgängligt i Tyskland efter 1949. Biochemie Kundl - nu var Sandoz / Novartis också involverad i forskning och spridning av penicillin (se filmen The Third Man ).
Tidigare arbete
Även nubianerna använde en öl med antibakteriella medel. De gamla egyptierna behandlade inflammationer med helande drycker bryggda av spannmål. I antiken och på medeltiden placerade kirurger mögliga trasor på sår för att förhindra infektion. De aktiva ingredienserna erkändes dock inte som sådana, termen antibiotikum introducerades bara med penicillinet.
Fleming var dock inte den första moderna forskaren som upptäckte att mögel kan hämma bakterietillväxt: Redan 1870 hade John Scott Burdon-Sanderson insett ett samband mellan mögel och bakterietillväxt. I 1884 behandlade Joseph Lister den abscess av en sjuksköterska med en Penicillium form (mer exakt, Penicillium glaucum ), resultat som inte publicerats. Ernest Duchesne genomförde ett framgångsrikt djurförsök med marsvin 1896 . Alla dessa fynd förblev emellertid utan resonans i den vetenskapliga världen och missuppfattades helt. Första Fleming använde säkert Penicillium notatum (som penicillin Burdon-Sanderson och Duchesne använde är tyvärr okänt).
Utveckling till genombrottet inom medicinsk praxis
Till en början fick Flemings publikationer lite uppmärksamhet från kollegor. Det var inte förrän andra världskriget som penicillin fick sitt genombrott. Det faktum att sulfonamiderna , varav en var det första antibiotikumet som användes i praktiken under handelsnamnet Prontosil , tillverkades i Tyskland och patenterades av tyska företag, så att de inte längre var tillgängliga på samma sätt för motståndarna till krig efter krigsutbrottet spelade en roll i detta. Det var bara i ytterligare forskning som fördelarna med penicillin G framför denna klass av aktiva ingredienser blev uppenbara. Tyskarna fortsatte dock att använda sulfonamider fram till krigsslutet.
1939 blev Howard Walter Florey och Ernst Boris Chain intresserade av penicillin. Norman Heatley lyckades extrahera och rena antibiotikumet från odlingsvätskan där formarna odlades. Den 24 augusti 1940 utfördes ett djurförsök på 50 råttor infekterade med en dödlig dos streptokocker . Hälften av dem fick penicillin, och bara en i den gruppen dog. Råttorna i den andra gruppen dog alla inom några timmar. Detta djurförsök avslöjade överraskande den kraftfulla effekten av penicillin, som inte förväntades med denna aggressiva bakteriestam.
Den 12 februari 1941 behandlades den första patienten med penicillinet som erhölls. Det handlade om den 43-årige London- polisen Albert Alexander, som skadades när han klippte en ros och drabbades av blodförgiftning från infektion av såret ; han injicerades med en dos på 160 milligram. Efter fem dagars behandling försvann febern , men penicillintillförseln var uttömd, varför behandlingen var tvungen att avbrytas. Patienten dog den 15 mars 1941.
Detta föreslog i efterhand att penicillinet borde ha tagits längre än de synliga symptomen kvarstår. Så vitt vi vet idag borde den första patienten ha behandlats i fem till tio dagar. En för tidig uppsägning medför alltid risken för ett återfall, även i dag ofta endast behandlingsbar genom användning av alternativa antibiotika.
Det var inte förrän Florey och Heatley flög till USA för att annonsera för penicillin som det allmänna intresset väcktes, särskilt bland den amerikanska militären. Det första steget var att leta efter en svampstam som producerade mer penicillin. För att göra detta samlade det amerikanska flygvapnet markprover från så många flygfält som möjligt runt om i världen. Den mest produktiva stammen, Penicillium chrysogenum , upptäcktes dock på en möglig melon framför forskningsinstitutet.
industriell produktion

Efter att "Oxford Circle" kring EB Chain och HW Florey hade publicerat en process för produktion och isolering av penicillin i " Lancet " 1940 och 1941, startades de första industriproduktionerna 1942, framför allt av Glaxo och ICI i England, MSD Sharp & Dohme (MSD), Pfizer & Co. och Squibb & Sons i USA och Schott Jena (driven av Hans Knöll ) i Tyskland.
År 1943 producerade läkemedelsföretag i USA nästan 1,5 ton rent penicillin, och 1945 kunde produktionen redan ökas till över 400 ton.
Från 1942 utfördes också forskning om penicillin vid Hoechst färgämnen (produktion i mindre skala började där våren 1945). Forskarna var tvungna att förlita sig på Flemings korta publikationer. Hoechst hade inte heller den rikliga Chrysogenum -stammen tillgänglig. Det var inte förrän 1950 som den amerikanska gruppen MSD skickade ett prov av denna stam till Västtyskland som en del av ett samarbete.
Samtidigt forskade Robert Thren på penicillinproduktion vid Madaus i Radebeul, Sachsen , varifrån östtysk produktion i läkemedelsfabriken i Dresden kom fram i samarbete med kemisten Alfred Kuhn . Som moderbolag till Pharmaceutical Combine GERMED levererades östblocket.
År 1945 var mängden penicillin som producerades i USA 20 gånger större än den som producerades i Europa. Vanlig majs , blötläggd i vatten, kallad majsstopplut av amerikanerna , visade sig vara det ideala näringsmediet för svampen. I processen (1944 vid Pfizer) ersattes ytprocessen (nedbrytningskultur) som ursprungligen användes av den nedsänkta processen (vätskekultur i en omrörd tankreaktor ), med vilken högre produktivitet uppnåddes. I oktober 1944 gjordes de första injektionspreparaten . År 1943 erbjöd 22 företag penicillin. Till en början var det huvudsakligen reserverat för sårade soldater, eftersom produktionsvolymen ännu inte var tillräcklig för att behandla alla civila patienter med det. Sedan 1944 har dock USA kunnat tillgodose alla sina civila och militära penicillinbehov. Å andra sidan, i Europa efter andra världskriget, var efterfrågan stor och penicillinproduktionen var inte tillräcklig för alla patienter. Smuggling och svarta marknaden handel med penicillin utvecklats, vilket också är föremål för filmen The Third Man .
Under årtiondena efter andra världskriget utvecklades Nederlandsche Gist-en Spiritusfabrik (NG & SF), senare Gist Brocades, idag DSM , till världens största penicillintillverkare. Idag producerar DSM penicilliner som en del av joint ventures i Folkrepubliken Kina , medan Sandoz GmbH i Kundl (Österrike) idag driver den största produktionsanläggningen för penicilliner i västvärlden.
Mänskliga prövningar
litteratur
- Charles R. Cramer: Om rengöring och kemi av penicilliner , Zürich 1949, DNB 570057728 (avhandling ETH Zurich 1949, 106 sidor).
- Christof Goddemeier: Alexander Fleming (1881–1955): Penicillin . I: Deutsches Ärzteblatt , volym 103, nr 36, 2006, s. A2286.
- Peter Imming: Hur gör svampen penicillin? Aktuell forskning, trender inom β-laktamantibiotika. Biosyntes av penicilliner och cefalosporiner. I: Pharmazie in our time , volym 18, nr 1, 1989, s. 20-24, doi: 10.1002 / pauz.19890180104 .
- Christian Mähr : Från alkohol till socker - tolv ämnen som förändrade världen. DuMont, Köln 2015, ISBN 978-3-8321-9549-6 .
- Ingrid Pieroth: Penicillinproduktion: från början till storskalig produktion (= Heidelberger Schriften zur Pharmazie- und Naturwissenschaftsgeschichte , Volume 9), Wissenschaftliche Verlagsgesellschaft , Stuttgart 1992, ISBN 3-8047-1248-7 (Dissertation University of Regensburg 1991, 168 sidor, under rubriken: Om historien om industriell penicillinproduktion från början till utvecklingen av storskalig produktion ).
- Vladimir Pliška: Penicillin och suilfonamid i kampen mot infektioner: mellan entusiasm och skepsis = La penicilline et les sulfonamides dans la lutte contre les infektioner: benediction ou malédiction (= BioFokus , Volym 24, nr 87), Association Research for Life, Zürich 2014, DNB 1049772873 (tyska och franska, fulltext (PDF) PDF, kostnadsfritt, 9 sidor, 1,6 MB).
- Barbara I. Tshisuaka: Penicillin. I: Werner E. Gerabek , Bernhard D. Haage, Gundolf Keil , Wolfgang Wegner (red.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4 , s. 1120.
- Susanne Krejsa MacManus: Penicillin från urinen. I: Deutsche Apotheker Zeitung , volym 160, nr 21, 21 maj 2020, s. 71–74
webb-länkar
- Biografi om Fleming (engelska)
- Fleming Nobel Prize Tal (PDF; 336 kB)
Individuella bevis
- ^ 6-aminopenicillansyra ; University of Hamburg, Institutionen för kemi.
- ↑ Penicilliner ( Memento från 24 april 2015 i Internetarkivet ): Byggstenar och metaboliska produkter, Urban & Fischer 2003 - Roche Lexicon Medicine, 5: e upplagan.
- ^ Michael T. Madigan, John M. Martinko, Jack Parker: Brock Microbiology. Tysk översättning redigerad av Werner Goebel, första upplagan. Spektrum Akademischer Verlag, Heidelberg / Berlin 2000, ISBN 3-8274-0566-1 , s. 440–441.
- ^ CE Higgens, RE Kastner: Streptomyces clavuligerus sp. nov., en β-laktamantibiotikaproducent. I: International Journal of Systematic and Evolutionary Bacteriology. Volym 21, nummer 4, oktober 1971, s. 326-331, doi: 10.1099 / 00207713-21-4-326 .
- ^ H. Cho, T. Uehara, TG Bernhardt: Betalaktamantibiotika inducerar en dödlig funktionsfel i syntesmaskineriet för bakterieceller. I: Cell. Volym 159, nummer 6, december 2014, s. 1300-1311, doi: 10.1016 / j.cell.2014.11.017 . PMID 25480295 .
- ↑ a b Britta Kasten, Ralf Reski : β-Lactam Antibiotics Inhibit Chloroplast Division in a Moss (Physcomitrella patens) men inte i Tomato (Lycopersicon esculentum) . I: J. Plant Physiol. , 1997, 150, s. 137-140 (engelska); Gratis fullständig textåtkomst ( Memento från 4 februari 2012 i Internetarkivet ; PDF)
- ↑ ÖÄZ v. 25 februari 2021, s. 3.
- ^ Erica S. Shenoy, Eric Macy, Theresa Rowe et al., Utvärdering och hantering av penicillinallergi: En översyn, https://pubmed.ncbi.nlm.nih.gov/30644987/
- ↑ Epileptiska anfall från antibiotika? ( Memento från 15 april 2018 i Internetarkivet ; PDF).
- ↑ Ernst Kern: Verkliga och förmodade framsteg inom kirurgi. I: Würzburg sjukdomshistoriska rapporter. Volym 9, 1991, sid. 417-429, här: s. 418.
- ↑ Dr. Clodomiro Picado Twight hedrad med WIPO -medalj (PDF). I: WIPO Magazine , s. 11. Hämtad 2 mars 2008.
- ↑ A. Fleming: Om den antibakteriella verkan av kulturer i ett penicillium, med särskild hänvisning till deras användning i isoleringen av B. influenzæ. Br J Exp Pathol 10 (3): sid. 226-236. (1929). PMC 2048009 (fri text)
- ^ HL Van Epps: René Dubos: avslöjar antibiotika . I: Journal of Experimental Medicine (JEM) , volym 203, 2006, S 259. doi: 10.1084 / jem.2032fta PMC 2118194 (fri text)
- ↑ Jonathan Wood: Penicillin: Oxford -historien . Oxford Science Blog, 16 juli 2010.
- ^ Alfred Marchionini , Hans Götz: Penicillinbehandling av hudsjukdomar. Springer-Verlag, Heidelberg 1950, s. 11 och 131.
- ↑ Florian G. Mildenberger : Ingen räddning genom arsenik? Salvarsandsdebatten och dess konsekvenser. I: Fachprosaforschung - Grenzüberreitungen , 8/9, 2012/2013, s. 327–390, här: s. 365.
- ↑ Ernst Kern : Seeing - Thinking - Agera av en kirurg på 1900 -talet. ecomed, Landsberg am Lech 2000. ISBN 3-609-20149-5 , s. 298.
- ^ Robert Bud: Penicillin - Triumf och tragedi . Oxford University Press, 2007, s. 51 books.google.de
- ^ Nobelpriset för medicin 1945. nobelprize.org
- ↑ Ernst Kern : Seeing - Thinking - Agera av en kirurg på 1900 -talet. ecomed, Landsberg am Lech 2000, ISBN 3-609-20149-5 , s. 198.
- ↑ Vem upptäckte penicillin - Fleming eller Lister? I: Läkartidningen , 9 november 2004
- ↑ David Wootton : Dålig medicin. Läkare gör skada sedan Hippokrates. Oxford, s. 248.
- ↑ a b c Martin Winkelheide : Den långa vägen till antibiotikumet. I: Kalenderblad (sänds på DLF ). 12 februari 2021, åtkomst 16 februari 2021 .
- ↑ Florian G. Mildenberger (2012/13), s. 365.
- ↑ I. Pieroth: Penicillinproduktion. Från början till storskalig produktion (Heidelberger Schriften zur Pharmazie- und Naturwissenschaftsgeschichte, volym 9). Vetenskapligt förlag, Stuttgart 1992, ISBN 978-3-8047-1248-5 .
- ↑ L. Marshall: I skuggan av kemisk syntes. Industriell bioteknik i Tyskland (1900–1970). Campus Verlag, Frankfurt 2000, ISBN 3-593-36585-5 .