Flavonoider
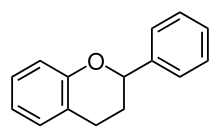
De flavonoider är en grupp av naturliga ämnen , till vilken en stor del av blompigment tillhör. Flavonoider tillhör gruppen polyfenoler . Formellt härrör de från den grundläggande strukturen Flavan (2-fenylkroman): två aromatiska ringar förbundna med en tetrahydropyranring . I naturen finns det cirka 8000 föreningar, vars mångfald skapas av olika oxidationstillstånd i den syreinnehållande ringen, olika substitutioner på de aromatiska ringarna och tillsatsen av sockerarter ( glykosidbildning ). Biosyntes sker via shikiminsyravägen .
Flavonoider är allmänt närvarande i växter som sekundära växtämnen , alltså också i livsmedel från människor. De sägs ha särskilt antioxidativa egenskaper. Ett antal växter som innehåller flavonoider används medicinskt.
Flavonoiderna upptäcktes på 1930-talet av Nobelprisvinnaren Albert von Szent-Györgyi Nagyrápolt och kallades ursprungligen vitamin P. "P" i vitamin P står för " permeabilitetsfaktor ".
Efternamn
Vissa växter, såsom färgerens ek ( Quercus tinctoria ), färgens växt ( Reseda luteola ) eller färgarens mullbärsträd ( Maclura tinctoria ) användes tidigare för gulning. Efter att ha identifierat deras ingredienser kallades denna grupp färgämnen flavoner, från det latinska ordet flavus för gul. När man insåg att många av ingredienserna är strukturerade på samma sätt, men har en annan färg eller är färglösa, kallades gruppen ämnen flavonoider.
Förekomst
Flavonoider är universellt fördelade i växtriket och förekommer i fröväxter samt mossor och ormbunkar . Bildningen av flavonoider är endast känd från några få mikroorganismer, såsom vattenkanna formar Aspergillus candidus . Djur kan inte göra flavonoider. Förekomsten hos vissa djurarter, till exempel i vingarna på vissa fjärilar , beror på intag av vegetabiliska flavonoider med mat och deras förvaring i kroppen. Enligt andra källor är flavonoiderna begränsade till växterna.
Struktur, mångfald och undergrupper
Den grundläggande strukturen hos flavonoiderna består av två aromatiska ringar som är förbundna med en C 3 bro. Ring A visar mestadels substitutionsmönstret för floroglucin , vilket indikerar dess ursprung i polyketidmetabolismen . Ring B och C 3 bron härrör från shikimisyra reaktionsvägen , är ringen B mestadels hydroxylerad vid 4', ofta också vid 3' eller 3 'och 5'. I den stora majoriteten av flavonoider (med undantag av chalconies ) den C 3 bron är stängd för att bilda en O-heterocyklisk ring (ring C). Den grundläggande strukturen för flavonoiderna är därför flavan (2-fenylchroman). Ring B flyttas sällan till position 3 (isoflavan, härledd från isoflavoner ) eller 4 (neoflavan).
Totalt har över 8000 olika flavonoider redan beskrivits (från och med 2006). Designen, särskilt graden av oxidation vid C 3- bron, tjänar till att dela upp flavonoiderna i de olika undergrupperna.
Sex huvudundergrupper finns i de flesta högre växter: Chalkoner , flavoner , flavonoler , flavandioler , antocyanidiner och kondenserade tanniner . De Aurons är mycket vanliga, men inte överallt. Isoflavoner (särskilt i Fabaceae ) och 3-deoxi-antocyanidiner, som bildas som föregångare till flobafener, till exempel av Vitis vinifera , Arachis hypogaea och Pinus sylvestris , är begränsade till några få grupper .
Den strukturella mångfalden av flavonoider beror på det stora antalet substitutionsmönster på ringarna A och B, liksom på det faktum att flavonoiderna vanligtvis inte är fria, utan snarare som glykosider . Över 80 olika sockerarter har identifierats. 179 olika glykosider har beskrivits för quercetin .
| Undergrupp | Grundläggande struktur | Exempel |
|---|---|---|
| Flavanoler |

|
Catechin , gallocatechin , epicatechin , epigallocatechin gallate |
| Flavanoler |

|
Taxifolin |
| Chalconies |

|
Isoliquiritigenin , xanthohumol (R2 = OH) |
| Antocyanidiner ( Anthocyaniner ) ("Flavenoler") |

|
Cyanidin , delfinidin , malvidin , pelargonidin , peonidin , petunidin (R3 = OH) |
| Flavonoler |

|
Morin , quercetin (glykosid rutin och metyleter isorhamnetin ), kaempferol , myricetin , fisetin |
| Aurone |

|
Aureusidin |
| Flavoner |

|
Luteolin , apigenin |
| Flavanones |

|
Hesperetin , naringenin , eriodictyol |
| Isoflavoner |

|
Genistein , Daidzein , Licoricidin |
biosyntes
Utgångspunkten för biosyntesen av flavonoiderna är den aromatiska aminosyran fenylalanin , som bildas via shikiminsyravägen . Fenylalanin omvandlas till trans - kanelsyra genom fenylalaninammoniaklyas (PAL) . Detta hydroxyleras i sin tur till p- minsyra med kanelsyra-4- hydroxylas. Denna väg är gemensam för alla fenylpropanoider . Den p -cumaric syra aktiveras för att ge kumaryl-koenzym A.
I nästa steg i den andra aromatiska ringen bildas: enzymet chalkonsyntas (CHS) bildas från cinnamoyl-CoA och tre molekyler av malonyl-coenzym A , bestående av fettsyrasyntes, kommer från chalkonen . Chalkon är i jämvikt med flavanon på grund av verkan av chalkonisomeras (CHI). Detta stänger den tredje ringen.
De tre nyckelenzymerna (PAL, CHS och CHI) liksom några av enzymerna i de ytterligare syntesstegen är närvarande som enzymkomplex . Komplexet ligger antagligen på den cytosoliska sidan av det endoplasmatiska retikulumet .
De olika vägarna leder från flavanon till flavoner, flavonoler, isoflavoner och antocyanidiner.
Biosyntesen av flavonoiderna induceras av ljus, lagringen sker huvudsakligen i vakuolen .
De flesta enzymerna för flavonoidbiosyntes kommer från tre klasser av enzymer som förekommer i alla organismer: oxoglutaratberoende dioxygenaser, NADPH-beroende reduktaser och cytokrom P450-hydroxylaser. De två nyckelenzymerna CHS och CHI tillhör olika familjer. CHI antas vara unik för växter både vad gäller sekvens och tredimensionell struktur. CHS tillhör i sin tur superfamiljen av vegetabiliska polyketidsyntaser .
betydelse
De olika flavonoiderna fyller en mängd funktioner i växter.

Flavonoider utgör den viktigaste gruppen bland blompigmenten och tjänar till att locka pollinatorer . Antocyanidinerna ger en mängd olika färger, allt från orange till rött till blått. Alla blommor innehållande antocyanidin innehåller också flavoner och / eller flavonoler, som tjänar till att stabilisera antocyanidinerna, men i högre koncentrationer får blommans färg också att flytta in i det blå området. Gul blommafärg orsakas mindre ofta av flavonoider. Flavonoler som gossypetin och quercetagetin är ansvariga för den gula blommans färg i Gossypium hirsutum , Primula vulgaris och vissa solrosväxter som Chrysanthemum segetum . Chalkoner och auroner är ansvariga för den gula blomman i vissa andra tusensköna växter som Coreopsis och Dahlia och i nio andra växtfamiljer. Gula flavonoider finns ofta i tusenskönafamiljen tillsammans med de gula karotenoiderna . 95% av den vita blommans färg orsakas av flavonoider: flavoner som luteolin och apigenin och flavonoler som kaempferol och quercetin , med flavonoler som absorberar något längre i långvågsområdet.
De kondenserade tanninerna interagerar med glykoproteinerna i växtätarnas saliv och har en sammandragande effekt . De minskar växternas smältbarhet och avskräcker därmed många potentiella växtätare.
Andra flavonoider fungerar som skydd mot växtätare ( repellanter ). För specialiserade insekter matar sådana flavonoider i sin tur stimulanser. I synnerhet är flavon- och flavonolglykosider, exempelvis baserade på rutin , quercitrin och isoquercitrin , giftiga för insekter, medan de är giftfria för högre djur. Tillväxten av olika larver reduceras dramatiskt i närvaro av till exempel isoquercitrin i kosten till 10% av kontrollgrupperna. Dessa flavonoider finns huvudsakligen i örtartade växter och bör ersätta träkornens kondenserade tanniner.
Speciellt flavoner och flavonoler fungerar som skydd mot UV-strålning och kortvågsbelysning. De deponeras i fri form av växter på extrema platser som i torra eller alpina områden på bladytan, ofta i form av mjölliknande beläggningar. På detta sätt förhindrar du fotooxidativ förstörelse av membran och fotosyntetiska pigment . På grund av deras lipofilicitet minskar de också koloniseringen av bladytan med mikroorganismer . Flavonoiderna har också direkta antivirala , antibakteriella och svampdödande effekter.
Vissa växt flavonoider spela en roll i regleringen av genuttryck i den knöl bakterien Rhizobium .
Mycket metoxylerade flavonoider finns ofta i utsöndringar från knoppar och andra lipofila sekret. De har en fungicid effekt , liksom nobiletinet i citrusblad .
Flavonoider fungerar som ett strukturellt tema i utvecklingen av selektiv GABA A- receptor - ligand .
Flavonoider i mat och medicin
mat
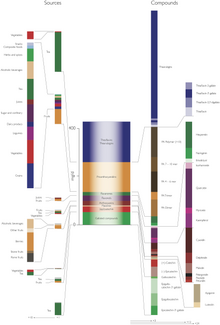
Människor får i sig stora mängder flavonoider med maten. Cirka två tredjedelar av de cirka ett gram fenolämnen som människor konsumerar varje dag är flavonoider. Huvudgruppen är flavanoler (speciellt i länder med tekonsumtion). Under lång tid har man antagit att den potentiella effekten av flavonoider är baserad på deras antioxidanteffekter, men detta tvivlas alltmer och andra verkningssätt är mer troliga.
Epidemiologiska studier har visat en lägre risk för olika sjukdomar med högre intag av flavonoider, inklusive dödlighet från hjärt-kärlsjukdom . Flavonoider verkar på arakidonsyrametabolismen och därmed på blodproppar. Olika studier (från och med 2016) visar att flavonoider också är direkt effektiva mot cancer eller dess utveckling.
Vissa föreningar har visat sig vara mutagena eller genotoxiska i in vitro-tester . Grönt te extrakt misstänks vara lever skada . En biverkning av ett läkemedel baserat på (+) - katekin som sedan dess har dragits ut från marknaden var hemolytisk anemi . Vidare misstänks flavonoider leda till för tidig tillslutning av ductus arteriosus .
Vissa flavonoider leder till en stark inhibering av cytokrom P450- beroende monooxygenaser (fas I-enzymer), andra leder i sin tur till en aktivering. En dosberoende aktivering av fas II-enzymer kan också förekomma. Allt detta kan leda till läkemedelsinteraktioner, såsom grapefrukt .
Farmaceutisk betydelse
Ett antal flavonoidinnehållande läkemedel används terapeutiskt, liksom vissa rena substanser. De används som venösa medel på grund av deras kärlskyddande, ödemskyddande effekt, som kardiovaskulära medel på grund av deras positiva inotropa , blodtryckssänkande effekt, som diuretika , som spasmolytika för gastrointestinala besvär och som leverterapi. Dess effekt tillskrivs främst dess antioxidativa egenskaper och hämningen av enzymer .
Epidemiologiska såväl som de flesta in vivo- studier indikerar att flavonoider har en positiv inverkan på olika hjärt-kärlsjukdomar . Traditionellt har dessa effekter endast tillskrivits deras antioxidantaktiviteter . Förutom den direkta bindningen av reaktiva syrearter (ROS) finns det dock ett antal andra effekter som i farmakologiskt uppnåbara koncentrationer också har en positiv effekt på kardiovaskulär påverkan av flavonoiderna såsom t.ex. B. Taxifolin kan vara ansvarig. Dessa inkluderar särskilt hämning av ROS-bildande enzymer, hämning av trombocytfunktion , hämning av leukocytaktivering och vasodilaterande egenskaper.
Bland de många effekterna av flavonoider som har visats i in vitro- och in vivo- test är de viktigaste:
- antiallergisk och antiinflammatorisk effekt
- antivirala och antimikrobiella effekter
- antioxidant effekt
- anti-proliferativa och cancerframkallande effekter
Flavonoider arbetar genom flera verkningsmekanismer. Fokus ligger på interaktionen med DNA och enzymer, aktivering av celler, deras egenskap som radikala borttagare och påverkan av olika signalöverföringsvägar i cellerna ( NF-KB , MAPK ). Flavonoider hämmar över trettio enzymer i människokroppen. De aktiverar en mängd olika celltyper i immunsystemet . De två sista egenskaperna är ansvariga för de antiinflammatoriska effekterna av flavonoider.
Följande flavonoider används som rena ämnen som venösa ämnen:
Bland läkemedlen dominerar de som innehåller flavonolglykosider och glykosylflavoner. Viktiga läkemedel som innehåller stora mängder flavonoider är:
- Arnica blommor ( Arnica )
- Björkblad ( silverbjörk , bogbjörk )
- Bovete ört ( Fagopyrum esculentum )
- Ginkgo Leaves ( Ginkgo )
- Goldenrod (från Solidago virgaurea , Solidago gigantea och Solidago canadensis )
- Elderflower ( svart fläderbär )
- Humlekottar ( äkta humle )
- Kamomillblommor ( kamomill )
- Cat's Paw Flowers ( Common Cat's Paw )
- Lärtextrakt ( Taxifolin )
- Meadowsweet ört och blommor ( meadowsweet )
- Mjölktistelfrukter ( mjölktistel )
- Passionsblommaört (från Passiflora incarnata )
- Bitter apelsinskal ( bitter orange )
- Marigold blommor ( ringblomma )
- Romersk kamomill
- Röda vinstockar ( Vitis vinifera )
- Safflorblommor ( safflor )
- Pansy ört ( Viola arvensis och Viola tricolor )
- Lakritsrot ( lakrits )
- Hagtorn lämnar med blommor (flera arter av hagtorn )
litteratur
- O. M. Andersen, KR Markham: Flavonoider: kemi, biokemi och applikationer . CRC Press, Taylor och Francis, Boca Raton 2006, ISBN 978-0-8493-2021-7 .
Individuella bevis
- ↑ St. Rusznyak, Albert Szent-Györgyi: P-vitamin: flavonoler som vitaminer. I: Natur. Volym 138, 1936, s.27.
- ↑ a b c d e f g h i j k Rudolf Hänsel , Otto Sticher (red.): Pharmakognosie. Fytofarmaci . 9: e upplagan. Springer Medizin Verlag, Heidelberg 2009, ISBN 978-3-642-00962-4 , s. 1098-1152.
- ↑ a b c d e f Martin Luckner: Sekundär metabolism i mikroorganismer, växter och djur . 3: e upplagan, VEB Gustav Fischer Verlag, Jena 1990, ISBN 3-334-00322-1 , s. 406-415.
- ↑ a b c Brenda Winkel-Shirley: Flavonoid biosyntes. En färgstark modell för genetik, biokemi, cellbiologi och bioteknik . I: Växtfysiologi. Volym 126, 2001, s. 485-493, doi: 10.1104 / s.126.2.485 .
- ↑ a b c d Bernhard Watzl, Gerhard Rechkemmer: Grundläggande kunskaper uppdaterade: Flavonoide. I: Nutrition review. Volym 48, nr 12, 2001 ( ernaehrungs-umschau.de ).
- ↑ a b c Hans-Walter Heldt : Växtbiokemi . Spektrum Akademischer Verlag, Heidelberg 1996, ISBN 3-8274-0103-8 , s. 423-437.
- ↑ Dieter Schlee: ekologisk biokemi . 2: a upplagan. Gustav Fischer Verlag, Jena 1992, ISBN 3-334-60393-8 , s. 67 f.
- ↑ a b J. B. Harborne: Introduktion till ekologisk biokemi . Tredje upplagan. Academic Press, London 1988, ISBN 0-12-324684-9 , s. 47-53.
- ^ JB Harborne: Introduktion till ekologisk biokemi . Tredje upplagan. Academic Press, London 1988, ISBN 0-12-324684-9 , s. 95, 175 f.
- ↑ Joseph Naghski, Michael J. Copley, James F. Couch: Den antibakteriella effekten av flavonoler. I: Journal of Bacteriology. Vol. 54, 34 (1947).
- ↑ Dieter Schlee: ekologisk biokemi . 2: a upplagan. Gustav Fischer Verlag, Jena 1992, ISBN 3-334-60393-8 , s. 271 f.
- ↑ JR Hanrahan, M. Chebib, GA Johnston: Flavonoidmodulation av GABA (A) -receptorer . I: Br J Pharmacol . 163, nr 2, 2011, s. 234–245. doi : 10.1111 / j.1476-5381.2011.01228.x . PMID 21244373 . PMC 3087128 (fri fullständig text).
- ↑ a b c Anna Vogiatzoglou, Angela A. Mulligan, Marleen AH Lentjes, Robert N. Luben, Jeremy PE Spencer: Flavonoidintag hos europeiska vuxna (18 till 64 år) . I: PLOS ONE . tejp 10 , nr. 5 , 26 maj 2015, s. e0128132 , doi : 10.1371 / journal.pone.0128132 ( plos.org [nås 15 augusti 2017]).
- ↑ Robert J. Williams, Jeremy PE Spencer, Catherine Rice-Evans: Flavonoider: antioxidanter eller signalmolekyler? I: Fri radikal biologi och medicin . tejp 36 , nr. 7 , s. 838–849 , doi : 10.1016 / j.freeradbiomed.2004.01.001 ( elsevier.com [nås 15 augusti 2017]).
- ↑ Anja Klappan: Påverkan av flavonoid quercetin på mTOR-signalvägen för livmoderhalsceller och bröstcancerceller . München 2014, DNB 1048361322 , urn : nbn: de: bvb: 19-165609 (avhandling, LMU München).
- ↑ Se också José Rueff et al.: Genetisk toxikologi av flavonoider: rollen av metaboliska tillstånd vid induktion av omvänd mutation, SOS-funktioner och systerkromatidutbyte. I: Mutagenes. Volym 1, nr 3, 1986, s. 179-183.
- ↑ Stephanie E. Martinez, Neal M. Davies, Jonathan K. Reynolds: Toxikologi och säkerhet för flavonoider . I: FLAVONOID FARMACOKINETICS . John Wiley & Sons, Inc., 2012, ISBN 978-1-118-46852-4 , pp. 249-280 , doi : 10.1002 / 9781118468524.ch6 .
- ↑ D. Shinkov, I. Urumov, N. Doĭchinova, V. Manolova, R. Ananieva: [Immun hemolytisk anemi orsakad av catergen] . I: Vutreshni Bolesti . tejp 28 , nr. 5 , 1989, sid. 84-87 , PMID 2618015 .
- ↑ Paulo Zielinsky, Stefano Busato: Prenatala effekter av moderns konsumtion av polyfenolrika livsmedel i sen graviditet vid fetal ductus arteriosus . I: Forskning om fosterskador Del C: Embryo idag: Recensioner . tejp 99 , nr. 4 , 1 december 2013, s. 256-274 , doi : 10.1002 / bdrc.21051 .
- ↑ P. Mladenka, L. Zatloukalová, T. Filipský, R. Hrdina: Kardiovaskulära effekter av flavonoider orsakas inte bara av direkt antioxidantaktivitet . I: Free Radic Biol Med . 2010, 49, s. 963-975, PMID 20542108 .