Spektral linje
Som spektrallinjer eller resonanslinjer , skarpt separerade linjer i ett spektrum av emitterade ( emissionslinjer ) eller absorberade ( absorptionslinjer ) av elektromagnetiska vågor , i smalare bemärkelse inom våglängdsområdet för synligt ljus ( ljusspektrum ). Spektrallinjer kännetecknas av våglängd , linjeintensitet och linjebredd . Orsaken till de spektrala linjerna är de ljusupphetsade elektroniska övergångarna iAtomer eller molekyler .
Namnet spektral linje går tillbaka historiskt på det faktum att det finns en ingång slits i konventionella spektrometrar , vars form reflekteras på skärmen eller i betraktarens öga. Namnet överfördes senare också till topparna (dvs. maxima) i ett spektrum registrerat som en intensitetskurva.
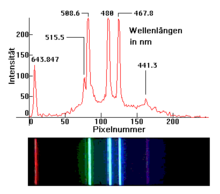
Spektrallinjer uppträder i instrumental atomspektroskopi (såsom kärnmagnetisk resonansspektroskopi ) eller i flamfärgning . De används bland annat i astronomi för att analysera den molekylära strukturen hos stjärnor , planeter och interstellär materia , vilket annars skulle vara omöjligt. De var i brytningen av ljus från solen genom ett prisma som upptäcktes på 1800-talet, från vilket spektroskop utvecklades som tillät ett brett användningsområde för spektralanalys .
Grunderna
En spektral linje är ljuset från en exakt definierad frekvens som emitteras (emitteras) eller absorberas (absorberas) av en atom eller molekyl på grund av en övergång från en energinivå till en annan. Frekvensen bestäms av energin hos den emitterade eller absorberade foton ; detta är lika med skillnaden mellan energierna i de två kvantmekaniska tillstånden . Frekvensen är karakteristisk för denna speciella övergång i den angivna typen av atom. Därför kan man skilja typer av atomer genom att observera spektrala linjer.
Utsläppslinje
En utsläppslinje dyker upp som en ljuslinje i spektrumet. Det uppstår under övergången från en högre till en lägre energinivå, till exempel när en elektron passerar från ett exciterat tillstånd till marktillståndet . Här avges en foton. Detta kan antingen hända spontant ( spontan emission ) eller, såsom. B. med laser , exciteras av ljus med en lämplig frekvens ( stimulerad emission ).
Absorptionslinje
När ljus bestrålas med ett kontinuerligt spektrum (dvs. en frekvensblandning), resulterar resonansabsorption av fotoner med en lämplig frekvens i en absorptionslinje i vilken en övergång från en lägre till en högre energinivå induceras - till exempel när en elektron passerar genom foton från valensbandet till Conduction-bandet "lyftes" (se fotoelektrisk effekt ).
När man faller tillbaka till den lägre energinivån blir fotoner isotropa , dvs. H. i någon riktning, släpps ut.
Båda dessa leder till att ljuset sprids diffus av materialet som bestrålas vid denna frekvens . Så länge det finns tillräckligt med absorberande atomer, kommer det till
- en mörk linje i det kontinuerliga spektrumet av ljus som lyser igenom ( Fraunhofer-linjen ); detta är vanligtvis vad som menas med termen absorptionslinje
- en ljus linje mot en mörk bakgrund vid analys av det spridda ljuset som kommer ut från gassidan; denna typ av ljuslinje kallas inte en utsläppslinje på grund av historisk terminologi ; Linjer kallas endast sådana om exciteringen inte gjordes med ljus med samma frekvens .
Utsläppsprofiler
Ljuset på en spektral linje innehåller inte en enda, skarpt definierad frekvens utan innehåller ett (smalt) frekvensområde. Den halvbredd av detta område kallas linjebredden . Linjebredden för en utsläppslinje består av flera bidrag:
- Lorentz profil
- Den naturliga linjebredden är resultatet av det ursprungliga tillståndets livstid genom Heisenbergs osäkerhetsprincip . Detta har formen av en Lorentz-kurva . Det går inte att minska detta.
- Gaussisk profil
- Atomernas termiska rörelse skapar en dopplereffekt som förskjuter ljuset från en enskild atom eller molekyl till rött eller blått, beroende på rörelseriktningen. Den statistiska rörelsen resulterar i en bredare frekvensfördelning totalt sett. Denna effekt kallas Doppler-breddning . Den har formen av en Gauss-kurva och är beroende av temperaturen . Vanligtvis dominerar dopplerbredden tydligt över den naturliga linjebredden. Mekanismen är också känd under termen inhomogen linjeutvidgning .
- Voigt-profil
- Under en mätning, att en Lorentz kurva av ändliga bredd visas ha ändrats från dess kända form om apparaten funktion av mätanordningen har en halv bredd i storleksordningen av Lorentz-kurvan under övervägande. Linjeformen kan sedan beskrivas genom faltning av Lorentz-kurvan och apparatens funktion. Om apparatfunktionen är en Gaussisk kurva kallas resultatet av fällningen en Voigt-profil .
historia
Absorptionslinjer upptäcktes först 1802 av William Hyde Wollaston och 1814, oberoende av honom, av Joseph von Fraunhofer i solens spektrum . Dessa mörka linjer i solspektrumet kallas också Fraunhofer-linjer .
De spektrala linjerna, bland andra effekter, bidrog till utvecklingen av kvantmekanik . Enligt klassisk elektrodynamik kan en elektron bunden i en atom avge elektromagnetiska vågor av vilken frekvens som helst; existensen av diskreta linjer kunde inte förklaras klassiskt. Upptäckten att frekvenserna för väteatomens spektrallinjer är proportionella mot ett uttryck av formen med heltal och ledde till begreppet kvantantal och slutligen förde Niels Bohr till sin Bohr-modell av atomen , den första - nu föråldrad - kvantmekanisk atommodell. Modern kvantmekanik kan förutsäga atommers spektrallinjer med mycket hög noggrannhet.
litteratur
- Heinz Haferkorn : Optik. Fysisk-tekniska grunder och tillämpningar. 4: e upplagan, Wiley-VCH 2003, ISBN 3-527-40372-8
- Ingolf Volker Hertel , Claus-Peter Schulz: Atomer, molekyler och optisk fysik 1 . Springer 2008, ISBN 978-3-540-30617-7
- Peter M. Skrabal: Spectroscopy , vdf Verlag, 2009, ISBN 978-3-8252-8355-1




